09 أكتوبر، 2019
الجزء الداخلي من بطارية ليثيوم
سلط منح جائزة نوبل للكيمياء لثلاثة من العلماء لدورهم في اكتشاف بطاريات الليثيوم، الضوء على هذا النوع من البطاريات الذي أحدث ثورة غيرت نمط حياتنا.
فبطاريات الليثيوم تستخدم على نطاق واسع من الأجهزة، من الهواتف النقالة والحواسيب المحمولة، إلى السيارات التي تعمل بالطاقة الكهربائية.
يقدر سوق بطاريات الليثيوم حاليا بأكثر من 90 مليار في العام، مقارنة بـ 37 مليار في عام 2018.
وتمتاز بطاريات الليثيوم بالقوة وهي تسهم في تحسين البيئة من خلال تقليل استخدام الوقود الأحفوري عبر السماح بتخزين الطاقة الشمسية وطاقة الرياح وغيرها من المصادر المتجددة.
وتم منح جائزة نوبل للكيمياء لعام 2019 للبريطاني ستانلي ويتينغهام، والأميركي جون غود إناف، والياباني أكيرا يوشينو الذين ساهموا في اختراع هذا النوع من البطاريات.
وقالت لجنة منح الجائزة على تويتر:
"من خلال عملهم (الثلاثة) وضع الحاصلون على جائزة نوبل للكيمياء هذا العام الأساس لمجتمع لاسلكي خال من الوقود الأحفوري".
The Nobel Prize
@NobelPrize
· ٩ أكتوبر ٢٠١٩
The 2019 #NobelPrize in Chemistry has been awarded to John B. Goodenough, M. Stanley Whittingham and Akira Yoshino “for the development of lithium-ion batteries.”
The Nobel Prize
@NobelPrize
Lithium-ion batteries have revolutionised our lives and are used in everything from mobile phones to laptops and electric vehicles. Through their work, this year’s Chemistry Laureates have laid the foundation of a wireless, fossil fuel-free society.#NobelPrize
٩ أكتوبر ٢٠١٩
https://twitter.com/NobelPrize/statu...%2F515378.html
أول بطارية
وطور ويتينغهام أول بطارية ليثيوم وظيفية في السبعينيات لكنها كانت شديدة الانفجار وغير قابلة للاستخدام.
ويتينغهام الذي يعمل في جامعة بينغهامبتون الأميركية، اكتشف مادة تسمى ثاني كبريتيد التيتانيوم قام بتوظيفها لإنتاج الطرف الموجب في البطارية ويسمى "الكاثود".
بعد ذلك قام بصنع "الأنود" (الطرف السالب) من الليثيوم المعدني المعروف جدا بإطلاقه للإلكترونات، وهو المعدن الأخف وزنا في الجدول الدوري للعناصر الكيميائية.
البطارية كانت بقدرة 2 فولت، لكن الليثيوم جعلها قابلة للانفجار.
غود إناف الأستاذ بجامعة تكساس قام في عام 1980 بتحسين أداء البطارية من خلال استخدام أكسيد الكوبالت بدلا عن الكبريتيتد، الأمر الذي رفع قدرة البطارية إلى 4 فولتات.
واستنادا لعمل غود إناف، ابتكر الياباني يوشينو أول بطارية ليثيوم قابلة للاستخدام التجاري في عام 1985. وهو يعمل الآن بجامعة ميجو اليابانية.
دخلت بطاريات الليثيوم السوق على نطاق واسع في عام 1991.
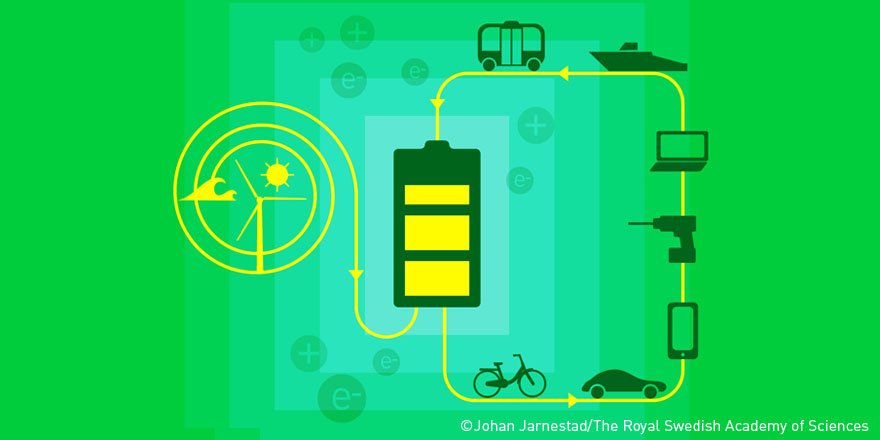
كيف تعمل؟
تقوم البطاريات بتخزين وإطلاق الطاقة بشكل أساسي من خلال سلسلة من التفاعلات الكيميائية التي تحدث عند قطبيها السالب (الأنود) والموجب (الكاثود).
تنتقل الأيونات الموجبة من الأنود إلى الكاثود من خلال محلول كهربائي (الكترولايت) موجود بين الاثنين.
ويتم عكس العملية لجعل البطارية قابلة للشحن.
ويعمل العلماء الآن على تطوير بطاريات ليثيوم بالكاربون ديوكسيد ويرى البعض أن هذا النوع سينقل تكنولوجيا البطاريات إلى مستوى جديد، بسبب طريقة إعادة شحنه وقدرته على الاحتفاظ بالطاقة لفترة طويلة.
النتائج 1 إلى 1 من 1
-

- تاريخ التسجيل
- May 2012
- اللقب
- عضو
- معدل المشاركات
- 0.43
- المشاركات
- 1,875
ما هي بطارية الليثيوم التي فاز مخترعوها بجائزة نوبل؟
معلومات الموضوع
الأعضاء الذين يشاهدون هذا الموضوع
الذين يشاهدون الموضوع الآن: 1 (0 من الأعضاء و 1 زائر)


 رد مع اقتباس
رد مع اقتباس
المفضلات